Sadržaj
- definicija
- Etilendiaminetetracetna kiselina i potenciometrijska metoda
- Složena geometrija
- Burette rješenje
Znanstvenici se oslanjaju na izravno titraciju kako bi pronašli količinu tvari u otopini s kemijskim reakcijama. Ako se ispravno izvodi, ovaj postupak može vrlo precizno prikazati kemijske količine pomoću specijaliziranih kiselina i laboratorijskog staklenog pribora. Da bi titracija radila ispravno, posljednji se kompleks mora oblikovati dovoljno brzo da bi ga znanstvenici mogli analizirati.
definicija
Izravno titranje način je kvantitativnog određivanja sadržaja neke tvari. Znanstvenici su možda svjesni reaktanata, ali ne znaju količine reaktanta. Izravno titranje ponekad se temelji na pokazateljima koji odgovaraju na analizirani materijal, nazvan analit. Druge se metode temelje na upotrebi dodanih iona metala, koji su pojedinačni atomi ili molekule određene vrste metala.
Etilendiaminetetracetna kiselina i potenciometrijska metoda
Tehničari mogu obavljati titraciju pomoću etilendiaminetetracetne kiseline s metal-ionskim pokazateljima. Ova metoda ne djeluje u svim situacijama, jer je reakcija ponekad toliko spora da titranje postaje nerealno. Korišteni metalni ion mora imati manju stabilnost od analita. Druga metoda izravne titracije je potenciometrijska metoda koja se koristi za detekciju krajnjih točaka s metalnim ionima koji imaju specifične raspoložive elektrode. Krajnja točka je točka gdje se završava postupak titracije.
Složena geometrija
Za kompleksometrijsku titraciju znanstvenici koriste aminopolikarboksilne kiseline za identifikaciju metala. Formiraju se obojeni kompleksi, a znanstvenici koriste prikupljene podatke iz te formacije kako bi odredili količinu analita. Izravna metoda kompleksometrijske titracije uključuje upotrebu otopine metala-soli titrirane otopinom složenih spojeva. Složene otopine sastojaka sadrže atome ili spojeve koji tvore komplekse s drugim atomima ili spojevima. Znanstvenici pronalaze točku ekvivalencije iz dodanog pokazatelja. Točka ekvivalencije je kada je dodani titrant stehiometrijski jednak analitu. Stehiometrija uključuje uravnoteženje kemijskih reakcija.
Burette rješenje
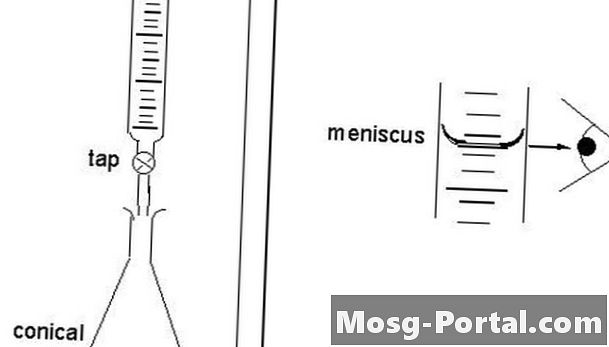
Izravno titranje naziva se "izravnim", jer znanstvenik izravno pristupa krajnjoj točki. Titran ulazi u otopinu kapljicama iz birete tako da konačni kap ne nadmaši krajnju točku. Izravnom titracijom znanstvenici tretiraju topljivu tvar koja se nalazi u otopini, a koja se nalazi u posudi koja se zove titrat. Standardizirana otopina naziva se titrant. Krajnja se točka određuje instrumentalno ili vizualno uz pomoć pokazatelja. Znanstvenici dodaju titran u ispravnu buretu, vertikalni i cilindrični komad staklenog posuđa s preciznom slavinom koja u određenim količinama ispušta male količine tekućine. Znanstvenici pune burete do 30 do 100 posto kapaciteta.